安科生物:PA3-17注射液纳入拟突破性治疗品种
记者近日从安科生物获悉,该公司参股的博生吉医药科技(苏州)有限公司、博生吉安科细胞技术有限公司自主研发的PA3-17注射液被国家药品监督管理局药品审评中心(CDE)纳入拟突破性治疗品种公示名单。
上证报中国证券网讯(记者 刘一枫)记者近日从安科生物获悉,该公司参股的博生吉医药科技(苏州)有限公司、博生吉安科细胞技术有限公司自主研发的PA3-17注射液被国家药品监督管理局药品审评中心(CDE)纳入拟突破性治疗品种公示名单。
据了解,PA3-17注射液是获得新药临床试验批准的靶向CD7的自体CAR-T细胞治疗产品,用于治疗成人复发/难治性T淋巴母细胞白血病/淋巴瘤(R/R T-ALL/LBL)。该药物于2021年8月获得《药物临床试验批准通知书》并已完成Ⅰ期注册临床试验,临床试验数据展现了显著的缓解率和可控的安全性,最佳客观缓解率(ORR)高达84.6%。
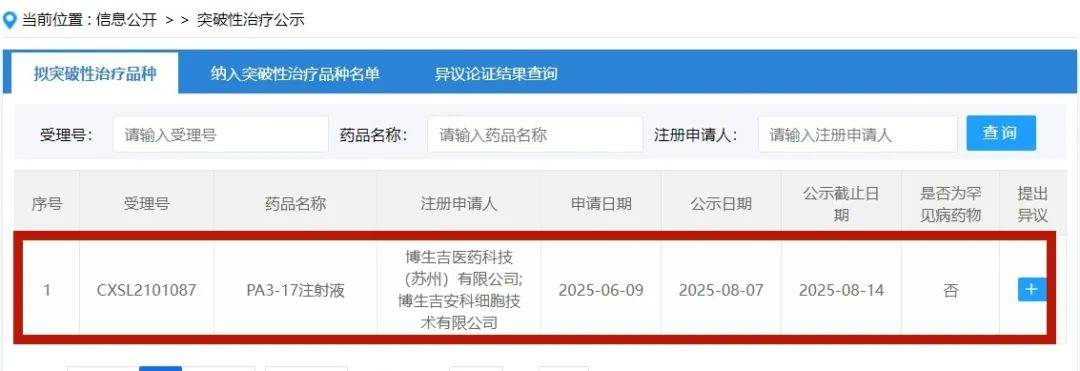
突破性治疗药物认定是CDE为加速具有显著临床优势的创新药物研发而设立的特殊审评通道,这一政策为“临床急需、疗效显著”的创新药提供了有力的支持。安科生物表示,PA3-17注射液纳入突破性治疗品种不仅能加速推动其上市进程,实现优先审评审批,更为中国原创细胞疗法走向全球竞争奠定坚实基础。
版权声明:如无特殊标注,文章均为本站原创,转载时请以链接形式注明文章出处。









评论